Изопропиловый спирт
Содержание:
- Токсичность
- Что такое пропан-1-ол
- Состав и способы производства
- Примеры решения задач
- Последствия
- Физические свойства
- Свойства [ править | править код ]
- Использование изопропанола
- Степень опасности и меры предосторожности
- Применение изопропанола в химической и автомобильной промышленности
- Получение [ править | править код ]
- Физико-химическая характеристика
- Токсикология
- Влияние на человека [ править | править код ]
- Применение
- Примечания
- 5. Применение
- Химические свойства
- Характерные свойства
- Применение изопропанола в других видах хозяйственной деятельности
Токсичность
Изопропанол применяется в медицине в качестве местного антисептика. При местном использовании быстро испаряется и не оказывает негативного влияния.
При вдыхании паров раздражает дыхательные пути, может вызвать головную боль. Высокая концентрация изопропанола в воздухе тормозит работу ЦНС, приводит к потере сознания. Поэтому работать с изопропанолом можно только в хорошо проветриваемом помещении.
Внутрь изопропанол не применяется, поскольку он токсичен. Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
Что такое пропан-1-ол
Пропан-1-ол представляет собой спирт, имеющий химическую формулу СН 3 СН 2 СН 2 ОН. Молярная масса этого спирта составляет 60, 1 г / моль. При комнатной температуре и давлении пропан-1-ол представляет собой бесцветную жидкость. Обладает умеренно-алкогольным запахом и характерным фруктовым ароматом. Температура плавления пропан-1-ола составляет -126, 1 ° С, а температура кипения составляет 97, 2 ° С.
При рассмотрении химической структуры пропан-1-ола, он имеет три атома углерода, связанных друг с другом, образуя основу молекулы. Поскольку соединение является насыщенным, не имеет двойных или тройных связей, все атомы углерода содержат четыре ковалентные связи вокруг них. Один из концевых атомов углерода связан с гидроксильной группой (-ОН). Все остальные облигации являются облигациями СН и СС. Следовательно, это первичный алкоголь.
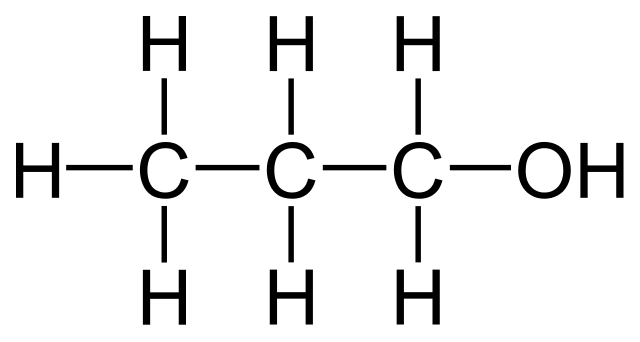
Рисунок 1: Химическая структура пропан-1-ола
Пропан-1-ол получают окислением алифатических углеводородов. Это соединение образуется в процессе ферментации, но в следовых количествах. Пропан-1-ол используется в качестве растворителя в таких отраслях, как фармацевтическая промышленность. Кроме того, этот спирт подходит для использования в качестве моторного топлива из-за его высокого октанового числа.
Состав и способы производства
Изопропиловый спирт (изопропанол, ИПС, диметикарбинол, 2-пропанол) – жидкое бесцветное химическое соединение с характерным запахом смеси спирта и ацетона. При пониженной температуре приобретает вязкую консистенцию. Обозначается молекулярной формулой С3Н8О. По химической характеристике – вторичный спирт алифатического ряда.
Физические и химические свойства вещества обусловили сферу его применения и меры предосторожности:
- растворим в эфире, хлороформе, алкогольсодержащих продуктах;
- при взаимодействии с металлами-окислителями легко превращается в ацетон;
- при сгорании распадается на углекислый газ и воду;
- температура замерзания 100% спирта -90 °С;
- хорошо соединяется с водой – чем больше спирта в растворе, тем ниже точка замерзания.
Вещество впервые было получено в 1920 году путем переработки нефтепродуктов. Сейчас промышленное производство осуществляется нескольким способами, чаще всего с помощью процесса гидратации – соединения воды и пропилена. От метода производства и вида сырья зависит степень чистоты конечного вещества.
Примеры решения задач
| Задание | Подвергнув анализу вещество, установили, что в его состав входят: натрий с массовой долей 0,4207 (или 42,07%), фосфор с массовой долей 0,189 (или 18,91%), кислород с массовой долей 0,3902 (или 39,02%). Найдите формулу соединения. |
| Решение | Обозначим число атомов натрия в молекуле через «х», число атомов фосфора через «у» и число атомов кислорода через «z». |
Найдем соответствующие относительные атомные массы элементов натрия, фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Ar(Na) = 23; Ar(P) = 31; Ar(O) = 16.
Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения:
Na:P:O = 42,07/39 : 18,91/31 : 39,02/16;
Na:P:O = 1,829 : 0,61 : 2,43.
Наименьшее число примем за единицу (т.е. все числа разделим на наименьшее число 0,61):
1,829/0,61 : 0,61/0,61 : 2,43/0,61;
Следовательно, простейшая формула соединения натрия, фосфора и кислорода имеет вид Na3PO4. Это фосфат натрия.
Ответ
Na3PO4
| Задание | Молярная масса соединения азота с водородом равна 32 г/моль. Определите молекулярную формулу вещества, массовая доля азота в котором составляет 85,7%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Вычислим массовую долю водорода в соединении:
ω (H) = 100% — ω(N) = 100% — 85,7% = 14,3%.
Обозначим количество моль элементов, входящих в состав соединения за «х» (азот), «у» (водород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
x:y= 6,12 : 14,3= 1 : 2.
Значит простейшая формула соединения азота с водородом будет иметь вид NH2 и молярную массу 16 г/моль [M(NH2) = Ar(N) + 2×Ar(H) = 14+ 2×1 = 14 + 2 = 16 г/моль].
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит индексы атомов азота и водорода должны быть в 2 раза выше, т.е. формула вещества будет иметь вид N2H4. Это гидразин.
Последствия
В употреблении изопропилового спирта опасно не только само отравление, но и возможные следующие реакции со стороны внутренних органов.
- Нарушение работы печени и почек.
- Проблемы системы пищеварения — развитие гастрита или язвенной болезни желудка и двенадцатипёрстной кишки.
- Возможно, появление параличей и других нарушений в работе нервной системы.
Опасен ли изопропиловый спирт? — да, как и любое другое химическое соединение. Но правильное его использование не приведёт к трагедии. А вот употребление жидкостей, содержащих изопропанол, вызовет серьёзное отравление и отдалённые последствия для здоровья.
Физические свойства
Многие свойства изопропанола, температура кипения например, обусловлены наличием спиртовой группы (-ОН). Эта группа обладает высокой полярностью. В результате чего группа –ОН одной молекулы изопропанола образует связь с группой –ОН другой молекулы изопропанола. Таким образом, молекулы ассоциируются, то есть соединяются между собой. Такую связь называют водородной. Она слабая, но имеет большое значение в природе.
Благодаря водородным связям вода H2O при обычных условиях — жидкость, а не газ, как, например, похожее по строению вещество H2S сероводород. Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.
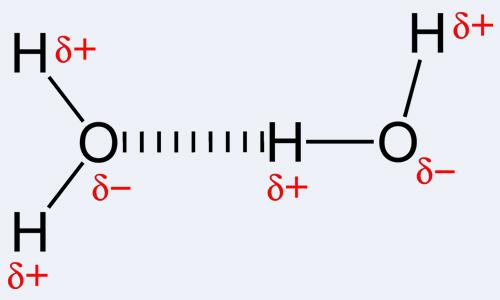
Образование водородных связей объясняет высокую температуру кипения изопропилового спирта и других низкомолекулярных спиртов в сравнении с соединениями схожего строения. Например, температура кипения пропана -42 °С, то есть пропан при любых температурах выше -42°С находится в газообразном состоянии. Температура кипения изопропилового спирта намного выше и составляет 82,4 °С. Это означает, что изопропанол при обычной температуре находится в жидком состоянии.
Если сравнить температуру кипения изопропилового спирта и метилового, то у первого она несколько выше: 82 градуса против 65. Это означает, что при обычных условиях изопропиловый спирт меньше испаряется, чем метиловый.
Температура плавления и температура кипения изопропилового спирта и некоторых других соединений представлены в таблице.
| Вещество | Температура кипения, о С | Температура плавления, о С |
| Метанол | 65 | -98 |
| Этанол | 78 | -117 |
| Пропанол | 97 | -127 |
| Изопропанол | 82 | -88 |
| Пропан | -42 | -190 |
Образование водородных связей между спиртовыми группами изопропанола и молекулами воды обуславливает растворимость этого спирта в воде. Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Свойства [ править | править код ]
Химические свойства
Рациональная химическая формула изопропилового спирта CH 3 CH ( OH ) CH 3 <displaystyle <ce >> и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон .
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким и приятным, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К) . Удельная теплота сгорания 34,1 МДж/кг .
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение :
| Концентрацияспирта, об % | Концентрацияспирта, вес. % | Температуразамерзания, °C |
|---|---|---|
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
Использование изопропанола
Изопропиловый спирт применяется в различных сферах человеческой деятельности. Среди них такие, как лакокрасочная промышленность, нефтепереработка, переработка древесины, химическая, парфюмерная и мебельная промышленность, автохимия.
При производстве лаков и красок он используется в качестве растворителя. В области нефтепереработки изопропиловый спирт нашел применение в качестве добавки к маслам и как растворитель.
При деревообработке его применяют для извлечения древесной смолы.
В химической и парфюмерной промышленности данное вещество используют как растворитель для эфиров и других веществ.
В сфере автохимии этот спирт нашел применение при производстве антифризов и других, требующихся для работы автомобилей, жидкостей.
 Изопропиловый спирт используют в парфюмерной промышленности
Изопропиловый спирт используют в парфюмерной промышленности
Изопропиловый спирт можно обнаружить в составе парфюмерии, косметики, бытовой химии, веществ для дезинфекции. Также его используют в слесарном деле.
Большая часть изопропилового спирта реализуется в процессе производства различных видов продукции. Его часто применяют в фармацевтическом деле, что связано с низкой токсичностью примесей. Некоторая часть изопропилового спирта используется в химии при получении ацетона. Однако чаще его применяют для получения изопропилбензола. Около 5 тонн в год используется в бытовых целях и в косметике.
Еще одним направлением использования изопропанола является включение его в состав бензина в качестве добавки.
Применение изопропанола в качестве растворителя
Изопропиловый спирт легко испаряется и обладает более низкой (в сравнении с другими растворителями) токсичностью. Как растворитель он подходит для многих составов. Все это обусловило активное использование этого спирта в качестве растворяющего и чистящего средства, особенно при очистке изделий от масляных загрязнений. Изопропиловый спирт можно применять для очистки деталей в электронной технике, клавиатуры, ЖК мониторов. Может быть неплохим вариантом в качестве чистящего средства в домашнем хозяйстве. Подойдет он для таких материалов, как ткань и древесина. В то же время его нельзя использовать для очистки винила.
Применение в химической промышленности и медицине
Изопропиловый спирт является сырьем для производства изопропилацетата, который также является растворителем. Реакция изопропанола с алюминием и четыреххлористым титаном приводит к выделению титана.
Изопропанол применяют в медицине в составе тампонов для дезинфекции, которые содержат водный раствор данного соединения. Также его используют в качестве осушающего средства в целях предотвращения появления наружного отита (одного из заболеваний ушей).
Использование изопропанола в автомобилестроении
Изопропанол используют в качестве основного ингредиента в составе топлива в целях растворения водной фракции в составе бензина. Это исключает риск замерзания воды. В продаже можно встретить аэрозольные баллончики, основное назначение которых – борьба с обледенением ветрового стекла. Также его используют для очистки тормозных систем от остатков тормозной жидкости.
Применение в биологии
Изопропиловый спирт используют как консервант для органики и для хранения анализов. Для консервации можно также использовать формальдегид, но он более токсичен.
Изопропанол нередко используют при исследованиях ДНК. Дело в том, что молекула ДНК не растворяется в этом спирте. В ходе исследований изопропиловый спирт добавляется в подготовленную ДНК в целях преципитирования.
Степень опасности и меры предосторожности
Изопропиловый спирт является огнеопасным веществом, поэтому любое взаимодействие с ним должно вестись при соблюдении правил безопасности. Хранить средство и работать с ним нужно вдалеке от отрытого пламени и источников высоких температур. Спирт легко смешивается с воздухом, при больших концентрациях образовывает взрывоопасный состав – работы с ним должны проводиться в хорошо проветриваемых помещениях.
Соединение относится к умеренно-опасным веществам по степени отравляющего действия на организм человека и должно храниться в недоступных для детей местах. Оно менее токсично, чем метанол и этиленгликоль. Случаи интоксикации встречаются очень редко – как правило, при намеренном употреблении внутрь.
Случайное отравление возможно при вдыхании паров во время манипуляций с большими объемами в непроветриваемом помещении.
Признаки интоксикации:
- тошнота,
- рвота,
- головокружение,
- потеря сознания,
- сильные мышечные боли.
Вещество не впитывается в организм через кожные покровы, но при постоянном взаимодействии с открытыми участками тела может вызвать химические ожоги. Однократное попадание на кожу негативных последствий, как правило, не вызывает. Недопустимо попадание соединения на слизистые оболочки и в глаза – опасны даже пары вещества, при работе с большим количеством изопропанола необходимо использовать средства защиты.
Изопропиловый спирт при условии его правильного применения – полезное и универсально вещество
Готовые препараты содержат безопасное количество изопропанола, при самостоятельном приготовлении растворов необходимо соблюдать осторожность, использовать защитные очки и перчатки для предупреждения несчастных случаев и отравления
Применение изопропанола в химической и автомобильной промышленности
Применение в химической промышленности следующее:
- сырье для производства ацетона,
- производство пластмасс – полиэтилена низкого давления и полипропилена,
- синтез изопропилацетата,
- производство инсектицидов,
- растворитель при производстве этилцеллюлозы, ацетилцеллюлозы, нитроцеллюлозы в лакокрасочной промышленности,
- безопасная транспортировка нитроцеллюлозы (в нее добавляют 30% изопропанола),
- экстрагент в тонкой химической технологии.
- применение в нефтеперерабатывающей промышленности:
- растворитель карбамида, применяемого для депарафинизации дизельного топлива,
- добавка к маслам, усиливающая их антикоррозионные свойства и понижающая температуру застывания,
- «удаление» воды из бензиновых баков.
Вода попадает в топливные магистрали и баки нефтебаз путем конденсации из влажного воздуха. При низких температурах она замерзает и может образовать ледяную пробку. При добавлении абсолютированного изопропанола вода в нем растворяется и не замерзает.
В автомобильной промышленности:
- «удаление» воды из бензобаков путем ее растворения,
- как компонент топлива для повышения октанового числа и уменьшения токсичных выбросов,
- антиобледенитель ветрового стекла,
- антифриз для радиаторов,
- удаление тормозной жидкости с гидравлических тормозных систем.

Получение [ править | править код ]
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена .
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
(CH3)2CHOSO2OH + H2O -> (CH3)2CHOH>>>»> CH 3 CH = CH 2 + H 2 SO 4 ⟶ ( CH 3 ) 2 CHOSO 2 OH + H 2 O ⟶ ( CH 3 ) 2 CHOH <displaystyle <ce (CH3)2CHOSO2OH + H2O -> (CH3)2CHOH>>> (CH3)2CHOSO2OH + H2O -> (CH3)2CHOH>>>»/> .
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата ( CH 3 ) 2 CHOSO 2 OH <displaystyle <ce <(CH3)2CHOSO2OH>>> , серной кислоты H 2 SO 4 <displaystyle <ce >> и воды H 2 O <displaystyle <ce >> . На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты H 3 PO 4 <displaystyle <<ce >>> на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами .
Современный способ гидрирования ацетона водородом:
C H 3 C O C H 3 + H 2 → k a t C H 3 C H ( O H ) C H 3 <displaystyle mathrm COCH_<3>+H_<2><xrightarrow >CH_<3>CH(OH)CH_<3>> > 3>
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора .
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск) и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск) .
Физико-химическая характеристика
Физические характеристики
| Молекулярная масса (усл. ед.) | 60,095 | Температура кипения (С) | 83 |
| Плотность пара по воздуху | 2,1 | Температура плавления (С) | -90 |
| Плотность (г/м3) | 0,78 | Температура разрушения (С) | |
| Скорость испарения (кг*с/м3) | Удельная теплота парообразования (кДж/кг) | ||
| Давление пара (мм рт.ст.) при ну | 33 | Удельная теплоёмкость жидкости (кДж/кг*С) | |
| Запах | спиртовой | Термостабильность |
Методы индикации
В воздухе: Фотометрический, реакция с персульфатом калия с образованием ацетона с последующим определением с салициловым альдегидом в щелочной среде, измеряемые концентрации 0,22-2,2 мг/куб.м. В воде: Газохроматографический, чувствительность 0,01 мг/л.
Токсикология
Употребление пропилового спирта, также как и этилового спирта, вызывает алкогольное опьянение. В организме человека пропиловый спирт окисляется до пропионовой кислоты, более едкой, чем уксусная кислота, в связи с чем токсичность пропилового спирта значительно выше, чем у этилового (ЛД50 для пропилового спирта 1870 мг/кг, для этилового спирта 7060 мг/кг). В то же время по сравнению с метиловым спиртом, ЛД50 которого составляет 1500 мг/кг, пропиловый спирт относительно безопасен.[источник не указан 154 дня]
ПДК пропилового спирта в воздухе рабочей зоны 10 мг/м3 (среднесменная за 8 часов) и 30 мг/м3 (максимально-разовая), в атмосферном воздухе населенных пунктов — не более 0,3 мг/м3.
По данным порог восприятия запаха мог достигать (среднее значение в группе) 540 и даже 25000 мг/м3; в работе — 660 мг/м3 (то есть в 66 (22) раза выше ПДКрз).
На 2011 год был зафиксирован один смертельный случай отравления пропиловым спиртом.
Влияние на человека [ править | править код ]
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает .
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей .
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко .
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов .
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием , наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола . Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть .
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Воняет она! Воняет!Нет возможности купить менее вонючую сторублёвую. Вот прикупил по случаю:

Смотрю состав:изопропил, гликоли, поверхностно активное вещество, бензоат натрия (тупо соль))), краситель, отдушка.

Сегодня в «Метро» смотрю — стоит ещё какая-то:

Смотрю состав: Деионизированная вода, пропан-2-ол, этиленгликоль, нанокомпонент.

А так — ничего личного — просто маркетинг!
И ещё. Помнится главной причиной замены метила на изопропил было то, что пьют незамерзайку проклятые алкаши! А сейчас не пьют и не травятся? Если раньше знали, что там метанол и пили, то теперь знают, что там другая отрава и не пьют? А этилен гликоль? Токсичен. Попадание этиленгликоля или его растворов в организм человека может привести к необратимым изменениям в организме и к летальному исходу. Не отрава?
Я вот что подумал — а нет варианта сделать незамерзайку самому из купленной водки и летней омывайки, да так, чтоб не замерзала? Химики есть? А то дышать этой отравой надоело!))))
Ну и напоследок — освежитель кофейно-ванильный)))):
Применение
1-Пропанол применяют в качестве растворителя для восков, полиамидных чернил, природных и синтетических смол, полиакрилонитрила; в производстве полиэтилена низкого давления; для получения карбометоксицеллюлозы; как обезжириватель металлов; сорастворитель поливинилхлоридных адгезивов; желатинирующий и пластифицирующий агент целлюлозноацетатных плёнок; алкилирующий агент. Его используют также для синтеза пропионовой кислоты, пропионового альдегида, пропилацетата, пропиламина, ПАВ, пестицидов, некоторых фармацевтических препаратов.
Топливо
1-Пропанол имеет высокое октановое число (118). Однако производство его слишком дорого для того, чтобы он стал широко применяемым топливом.
Примечания
- Yaws, CL Chemical Properties Handbook. — McGraw-Hill, 1999.
- М. Вегthеlоt, Ann. Chim. et phys., 43, № 3, 391 (1855).
- Doolittle, Arthur K. (1954). The Technology of Solvents and Plasticizers. New York: John Wiley & Sons, Inc .. p. 628.
- ↑ The Merck Index (10th ed.). Rahway, NJ: Merck & Co .. 1983. p. 749.
- Патенты США 1725083, 1927 и 2420998, 1947.
- Английские патенты 293015, 1928 и 401284, 1932.
- Французский патент 743530, 1932.
- F. Asingег, Chemie und Technologie der Monoolefine, Berlin, 1957, S. 581-584.
- IG Park, С. М. Вeamer, in Kirk — Оthmer, Encyclopedia of Chemical Technology, v. 11, NY, 1953, p. 185-187.
- Патент США 2473224, 1949.
- W. Н. Shiffleг et al., Industrial & Engineering Chemistry, 31, 1101 (1939).
- Itakura T., Journal of the Chemical Society of Japan, 63, 1400 (1942).
- Reynolds PW, Grudgings DM, английский патент 622937, 10 мая 1949
- Ozol RJ, Masterson CR, патент США 2356689, 22 августа 1944.
- Frejacques JLM, патент США 2461048, 8 февраля 1949.
- Maryott AA, Journal of the American Chemical Society, 63, 3079 (1941).
- Mathews JH, Journal of the American Chemical Society, 48, 562 (1926).
- Lebo RB, Journal of the American Chemical Society, 43, 1005 (1921)
- Herold W., Wolf KL, Zeitschrift f?r Physikalische Chemie, 12B, 194 (1931).
- Gilson LE, Journal of the American Chemical Society, 54, 1445 (1932)
- Young, W.; Hartung, W.; Crossley, F. (1936). «Reduction of Aldehydes with Aluminum Isopropoxide». J. Am. Chem. Soc. 58: 100-2.
5. Применение
Основное количество изопропилового спирта используется для получения ацетона, однако она уменьшается из-за серьезной конкуренции со стороны кумольного метода производства ацетона.
Изопропиловый спирт распространен как растворитель для жиров, натуральных и синтетических смол, нитролаков (в сочетании с другими растворителями), алкалоидов, протеинов, хлорофилла и других веществ. Он используется и как составная часть детергентов (жидкие мыла).
Наряду с применением для синтеза ацетона изопропиловый спирт используют для синтеза различных сложных эфиров (например, изопропилацетата — растворителя лаков), для введения изопропилового группы в другие соединения (тимол, изопропилфенол). Ксантогенат изопропилового спирта является важным флотационным агентом. Изопропилата алюминия применяют для восстановления альдегидов методом Меервейна-Понндорфа.
Изопропиловый спирт заменяет этиловый во многих косметических и фармацевтических препаратах. Но он пригоден только для наружного применения, например дезинфекции. Применение его для лекарств и пищевых продуктов запрещено.
В большом количестве изопропиловый спирт используется для улучшения качества топлива. В карбюраторе двигателя при температуре от -8 до +13 ? С и относительной влажности воздуха 60-100% может наступить обледенение, что затрудняет запуск и выключение двигателя. Для устранения этого нежелательного явления достаточно добавить к бензину 1,5-3% изопропилового спирта.
Изопропиловый спирт используют для предотвращения обледенения крыльев и пропеллеров самолетов, а смесь этиленгликоля и изопропилового спирта устраняет обледенения стартовых дорожек и взлетно-посадочных полос на аэродромах.
Химические свойства
Пропиловый спирт обладает всеми химическими свойствами первичных одноатомных спиртов. Так он может быть превращён в галогеналканы: взаимодействие с йодом и красным фосфором даёт 1-йодпропан с 80 % выходом, тогда как взаимодействие хлорида фосфора (III) при катализе хлоридом цинка либо хлористого тионила при катализе ДМФА даёт 1-хлорпропан.
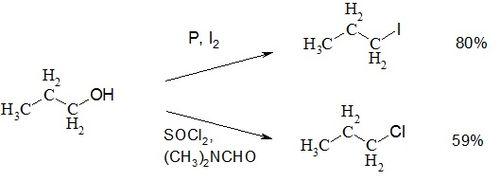
Реакция 1-пропанола с уксусной кислотой в присутствии серной кислоты даёт пропилацетат. В то время как кипячение только с муравьиной кислотой в течение суток даёт пропилформиат с выходом 65 %.
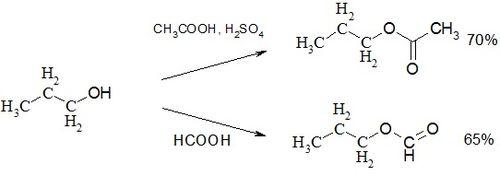
Окисление бихроматом калия с серной кислотой в условиях отгонки образующего пропаналя позволяет получать его с выходом 50 %. Более глубокое окисление хромовым ангидридом даёт пропионовую кислоту.
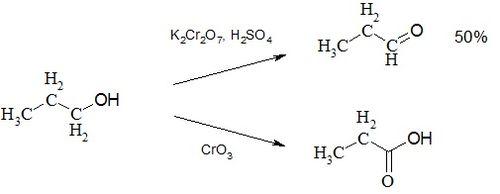
Взаимодействие со щелочными металлами даёт соответствующие пропиолаты металлов. Причём реакция протекает менее интенсивно чем с этиловым спиртом и намного менее интенсивно чем с водой.
-
- 2CH3CH2CH2OH+2Na→2CH3CH2CH2ONa+H2{\displaystyle {\mathsf {2CH_{3}CH_{2}CH_{2}OH+2Na\rightarrow 2CH_{3}CH_{2}CH_{2}ONa+H_{2}}}}
Характерные свойства
Характеристики изопропилового спирта мало чем отличаются от иных спиртовых веществ. Из них выделяются следующие свойства изопропила:
- Формула вещества с3 h 8о (абсолютированный элемент). В сочетании с водородом можно получить ацетон. Может взаимодействовать с пластиком и резиной.
- Прозрачная субстанция самовоспламеняется при температуре от 440 градусов. Изопропаноловые пары при кипении перемешиваются с кислородом, образуя газ, который опасен при любых вспышках и искрах пламени. Растворить изопропил можно в бензоле или ацетоне, так как он имеет низкую молярную массу. Если он присутствует в составе воды, то может и замерзать.
Именно эти свойства позволяют использовать вещество во многих сферах, как и этиловый спирт. Так или иначе, но при работе с ним нужно проявить максимальную внимательность, так как эти соединения трудно отличить.
Применение изопропанола в других видах хозяйственной деятельности
Применение в мебельной и лесохимической промышленности:
- экстракция смол из древесины в смеси с другими растворителями,
- снятие старого лакового покрытия, растворитель французской полировки, клеев, масел,
- связующее вещество в полиролях и очистителях.
В полиграфии изопропанол применяют для увлажнения в печатных процессах. В электронике — в качестве растворителя для очистки контактных разъемов, магнитных лент, головок дисков, лазерных линз, для удаления термопасты, очистки клавиатуры, ЖК-мониторов, стеклянных экранов. Нельзя применять его только для очистки винила, так как изопропанол вступает с ним в реакцию.
Применение в медицинской промышленности и медицине:
- входит в состав антисептических растворов, пропитывающих жидкостей для салфеток,
- обеззараживающее средство для протирания места инъекции,
- 75% водный раствор используют как дезинфицирующее средство для рук,
- дезинфицирующие тампоны,
- осушитель для профилактики отита,
- консервирующее средство для сохранения генетического материала и анализов (менее токсичен, чем формальдегид).
Изопропанол имеет преимущества перед этанолом: более выраженное антисептическое действие и низкую цену. Поэтому в тех случаях, когда раньше применяли этанол, сейчас используют изопропанол.
В косметической и парфюмерной промышленностях изопропанол применяют в производстве:
- косметических средств,
- средств личной гигиены,
- духов, одеколонов, лаков.
В пищевой промышленности изопропанол используют при производстве замороженных продуктов в качестве хладоносителя.
В домашнем хозяйстве:
- для очищения различных поверхностей, кроме резиновых и виниловых,
- для удаления пятен с тканей, древесины,
- для удаления клея от наклеек (на бумажные изопропанол не действует).