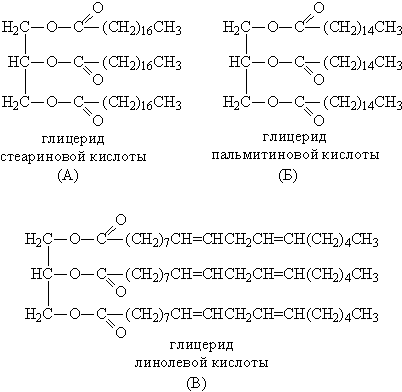
Фосфорноватистая кислота
Содержание:
Строение
Пары оксида фосфора(V) имеют состав P4O10. Твердый оксид склонен к полиморфизму. Существует в аморфном стекловидном состоянии и кристаллическом. Для кристаллического состояния известны две метастабильные модификации пентаоксида фосфора — гексагональная Н-форма (а = 0,744 нм, = 87°, пространств, гр. R3С) и орторомбическая О-форма (а = 0,923 нм, b = 0,718 нм, с = 0,494 нм, пространств, гр. Рпат), а также одна стабильная орторомбическая О-форма (а =1,63 нм, b= 0,814 нм, с =0,526 нм, пространств. гр. Fdd2). Молекулы P4O10 (Н-форма) построены из 4 групп PO4 в виде тетраэдра, вершины которого занимают атомы фосфора, 6 атомов кислорода располагаются вдоль ребер, а 4 — по оси третьего порядка тетраэдра. Эта модификация легко возгоняется (360°С) и активно взаимодействует с водой.
Другие модификации имеют слоистую полимерную структуру из тетраэдров PO4, объединенные в 10-членные (О-форма) и 6-членные (О’-форма) кольца. Эти модификации имеют более высокую температуру возгонки (~580°С) и менее химически активны. H-форма переходит в О-форму при 300—360оC.
Свойства
H3PO4 — трёхосновная кислота средней силы. При взаимодействии с очень сильной кислотой, например, с хлорной HClO4, фосфорная кислота проявляет признаки амфотерности — образуются соли фосфорила, например [Р(ОН)4]ClO4.
В водных растворах подвергается электролитической диссоциации в три стадии с образованием катиона гидроксония. Степень диссоциации и вид зависят от pH раствора:
-
H3PO4(aq)+H2O(l)⇌{\displaystyle {\mathsf {H_{3}PO_{4(aq)}+H_{2}O_{(l)}\rightleftharpoons }}} H3O(aq)++H2PO4(aq)−{\displaystyle {\mathsf {H_{3}O_{(aq)}^{+}+H_{2}PO_{4(aq)}^{-}}}} Ks1=6,9⋅10−3{\displaystyle {\mathsf {K_{s1}=6,9\cdot 10^{-3}}}} H2PO4(aq)−+H2O(l)⇌{\displaystyle {\mathsf {H_{2}PO_{4(aq)}^{-}+H_{2}O_{(l)}\rightleftharpoons }}} H3O(aq)++HPO4(aq)2−{\displaystyle {\mathsf {H_{3}O_{(aq)}^{+}+HPO_{4(aq)}^{2-}}}} Ks2=6,2⋅10−8{\displaystyle {\mathsf {K_{s2}=6,2\cdot 10^{-8}}}} HPO4(aq)2−+H2O(l)⇌{\displaystyle {\mathsf {HPO_{4(aq)}^{2-}+H_{2}O_{(l)}\rightleftharpoons }}} H3O(aq)++PO4(aq)3−{\displaystyle {\mathsf {H_{3}O_{(aq)}^{+}+PO_{4(aq)}^{3-}}}} Ks3=4,7⋅10−13{\displaystyle {\mathsf {K_{s3}=4,7\cdot 10^{-13}}}}
Отличительной реакцией ортофосфорной кислоты от других фосфорных кислот является реакция с нитратом серебра, при этом образуется жёлтый осадок:
- H3PO4+3AgNO3→Ag3PO4+3HNO3{\displaystyle {\mathsf {H_{3}PO_{4}+3AgNO_{3}\rightarrow Ag_{3}PO_{4}+3HNO_{3}}}}
Качественной реакцией на ион H2РО4− является образование ярко-жёлтого осадка молибденофосфата аммония:
- H3PO4+12NH42MoO4+21HNO3→NH43PMo12O40⋅6H2O↓+21NH4NO3+6H2O{\displaystyle {\mathsf {H_{3}PO_{4}+12_{2}MoO_{4}+21HNO_{3}\rightarrow _{3}PMo_{12}O_{40}\cdot 6H_{2}O\downarrow +21NH_{4}NO_{3}+6H_{2}O}}}
Степень диссоциации ортофосфорной кислоты в зависимости от кислотности раствора.
Свойства
P4O10 очень активно взаимодействует с водой (H-форма поглощает воду даже со взрывом), образуя смеси фосфорных кислот, состав которых зависит от количества воды и других условий:
-
- P4O10+6H2O→4H3PO4{\displaystyle {\mathsf {P_{4}O_{10}+6H_{2}O\rightarrow 4H_{3}PO_{4}}}}
При сильном нагревании распадается на:
-
- P4O10→P4O6+2O2{\displaystyle {\mathsf {P_{4}O_{10}\rightarrow P_{4}O_{6}+2O_{2}}}}
Он также способен извлекать воду из других соединений, представляя собой сильное дегидратирующее средство:
-
- 4HNO3+P4O10→4HPO3+2N2O5{\displaystyle {\mathsf {4HNO_{3}+P_{4}O_{10}\rightarrow 4HPO_{3}+2N_{2}O_{5}}}}
-
- 4HClO4+P4O10→(HPO3)4+2Cl2O7{\displaystyle {\mathsf {4HClO_{4}+P_{4}O_{10}\rightarrow (HPO_{3})_{4}+2Cl_{2}O_{7}}}}
Оксид фосфора(V) широко применяется в органическом синтезе. Он реагирует с амидами, превращая их в нитрилы:
-
- P4O10+RCONH2→P4O9(OH)2+RCN{\displaystyle {\mathsf {P_{4}O_{10}+RCONH_{2}\rightarrow P_{4}O_{9}(OH)_{2}+RCN}}}
Карбоновые кислоты переводит в соответствующие ангидриды:
-
- P4O10+12RCOOH→4H3PO4+6(RCO)2O{\displaystyle {\mathsf {P_{4}O_{10}+12RCOOH\rightarrow 4H_{3}PO_{4}+6(RCO)_{2}O}}}
Оксид фосфора(V) также взаимодействует со спиртами, эфирами, фенолами и другими органическими соединениями. При этом происходит разрыв связей P—О—P и образуются фосфорорганические соединения. Реагирует с NH3 и с галогеноводородами, образуя фосфаты аммония и оксигалогениды фосфора:
-
- P4O10+8PCl3+O2→12POCl3{\displaystyle {\mathsf {P_{4}O_{10}+8PCl_{3}+O_{2}\rightarrow 12POCl_{3}}}}
При сплавлении P4O10 с основными оксидами образует различные твёрдые фосфаты, природа которых зависит от условий реакции.
Химические свойства
На свету или при нагревании в вакууме разлагается с выделением красного фосфора:
-
- 4P4O6 →hν 3P4O8+4P{\displaystyle {\mathsf {4P_{4}O_{6}\ {\xrightarrow {h\nu }}\ 3P_{4}O_{8}+4P}}}
Медленно реагирует с холодной водой:
-
- P4O6+5H2O → 2H2(PHO3)+H2(P2H2O5){\displaystyle {\mathsf {P_{4}O_{6}+5H_{2}O\ {\xrightarrow {}}\ 2H_{2}(PHO_{3})+H_{2}(P_{2}H_{2}O_{5})}}}
и быстро с горячей водой:
-
- 6P4O6+24H2O → 8P↓+15H3PO4+PH3↑{\displaystyle {\mathsf {6P_{4}O_{6}+24H_{2}O\ {\xrightarrow {}}\ 8P\downarrow +15H_{3}PO_{4}+PH_{3}\uparrow }}}
Реагирует со щелочами:
-
- P4O6+6NaOH → 2Na2(PHO3)+Na2(P2H2O5)+H2O{\displaystyle {\mathsf {P_{4}O_{6}+6NaOH\ {\xrightarrow {}}\ 2Na_{2}(PHO_{3})+Na_{2}(P_{2}H_{2}O_{5})+H_{2}O}}}
Окисляется кислородом воздуха (быстрее при нагревании):
-
- P4O6+2O2 →50−120oC P4O10{\displaystyle {\mathsf {P_{4}O_{6}+2O_{2}\ {\xrightarrow {50-120^{o}C}}\ P_{4}O_{10}}}}
Реагирует с галогенами:
-
- P4O6+6Cl2 → 4PCl3O+O2{\displaystyle {\mathsf {P_{4}O_{6}+6Cl_{2}\ {\xrightarrow {}}\ 4PCl_{3}O+O_{2}}}}
Реагирует с серой:
-
- P4O6+9S → P4S6+3SO2{\displaystyle {\mathsf {P_{4}O_{6}+9S\ {\xrightarrow {}}\ P_{4}S_{6}+3SO_{2}}}}
Дифосфорная кислота
Дифосфорная кислота более сильная, чем ортофосфорная.
|
Структуры дифосфорной кислоты ( а, цепочечных и циклических фосфатов ( б. |
Дифосфорная кислота является более сильной, чем ортофосфорная, в соответствии с общим правилом увеличения силы кислот при их конденсации.
Пирофосфорная кислота ( дифосфорная кислота, Н4Р2О7) образуется при регулируемом нагревании ортофосфорной кислоты. Она неустойчива на влажном воздухе и легко превращается в фосфорную кислоту.
|
Механизм воспроизведения дезоксирибонуклеиновой кислоты Ad — аденин. Ci — цитовин. Т1 — тимин. Gu — гуанин. |
Сырьем служат нуклеозид-5 — дифосфорные кислоты ( см. ниже), соединяющиеся друг с другом с отщеплением фосфорной кислоты и образованием полинуклеотида.
Диспрозий 46, 50, 604 Дитионаты 459 Дитионистая кислота 449 Диуранаты 609 Дифосфин 415 Дифосфорная кислота 419 Дифторамин 433 Дифтордиазин.
В данную товарную позицию включаются оксид фосфора, фосфорная кислота ( ортофос-форная кислота или обыкновенная фосфорная кислота), дифосфорная кислота, полиметафос-форная и другие полифосфорные кислоты.
Если обогатить молекулу остатком второй молекулы ортофосфорной кислоты, получается АДФ или аденозиндифосфорная кислота, являющаяся уже замещенной пиро — или дифосфорной кислоты.
Кислоты, содержащие свыше одного атома кислотообразующего элемента в одной и той же степени окисления, называются изополи-кислотами; число атомов этого элемента указывают русской или греческой приставкой, например Н4Р2О7 — дифосфорная кислота.
Дальтона закон 209 Дейтерий 454 Дентатность 125 Диаграмма состояния 307 — 314 Дигидрофосфаты 417 Дисерная кислота 444 Дисернистая кислота 441 Диспрозий 50, 52, 571 Дисульфаты 444 Дитионаты 449 Дитионистая кислота 441 Дифосфорная кислота 418 Дифторамин 428 Дифтордиазин 428 Дихроматы 515 ел.
Дальтона закон 209 Дейтерий 454 Дентатностъ 125 Диаграмма состояния 307 — 314 Дигидрофосфаты 417 Дисерная кислота 444 Дисериистая кислота 441 Диспрозий 50, 52, 571 Дисульфаты 444 Дитионаты 449 Дитионистая кислота 441 Дифосфорная кислота 418 Дифторамин 428 Дифтордиаэин 428 Дихроматы 515 ел, 521 Дициак ( циан) 371 ел.
Составьте формулы соединений по их названиям: гидрид кальция, пероксид водорода, супероксид цезия, хлорид аммония, тетраборат натрия ( бура), оксохлорид хрома, гидрид мышьяка ( III), дифосфорная кислота.
Для получения изопропилбензола как высокооктанового компонента авиационного бензина применяют твердый фосфор-нокислотный катализатор. Алкилирование ведут в трубчатом реакторе на катализаторе, содержащем дифосфорную кислоту, нанесенную на кизельгур. Внизу реактора находится решетка, на которую слоем высотой примерно 5 м загружен катализатор. Для проведения процесса устанавливают последовательно несколько реакторов, в которые пропилен подают ступенчато. Смесь бензола и про-пан-пропиленовой фракции при мольном соотношении пропилен: бензол, равном ( 1 3ч — 3 5): 1, пропускают через слой катализатора с объемной скоростью 3 5 ч — при 225 — 250 С и 2 5 МПа. Теплота реакции при 250 С составляет 98 кДж / моль. Катализатор работает в течение 700 — 800 ч, затем теряет активность, и его заменяют свежим.
Результаты испытаний на шестеренном стенде FZG показывают, что трикрезилфосфат по эффективности уступает трибутил-фосфату. Эффективность трикрезилфосфата может быть повышена введением небольших количеств олеиновой кислоты. Наряду с кислотными и нейтральными алкил — и арилфосфатами, например трифенилфосфатом, триолеилфосфатом и др., среди которых алкилфосфаты превосходят арилфосфаты по эффективности, в качестве противозадирных присадок рекомендованы диалкил-фосфаты, бутилфосфонат, эфиры дифосфорной кислоты и триал-килфосфины; некоторые из них характеризуются высокой термической стабильностью. Среди триарилфосфатов фенил — и крезил-производным придается особое значение; о-крезол из-за его токсичности следует исключать.
Химические свойства
Фосфор в PCl3 находится в степени окисления +3, а хлор — в степени −1. Многие из свойств соединения обусловлены именно этими обстоятельствами. В присутствии воды — дымит и разлагается.
PCl3 — базовый продукт для других производных фосфора, получаемых из него при окислении до пентахлорида(PCl5), тиофосфорилхлорида (PSCl3) или оксихлорида (POCl3).
Если пропустить электрический разряд через смесь пара PCl3 и газообразного водорода, образуется редкий сложный хлорид фосфора с формулой P2Cl4.
Известно большое число сходных реакций замещения, в том числе и с органическими веществами — спиртами и фенолами:
Спирты реагируют сходным образом:
Наличие неподелённой электронной пары у атомов фосфора обуславливает способность трихлорида проявлять донорные свойства, образуя электронейтральные комплексы, например, [Ni(PCl3)4] По химической природе трихлорид фосфора является хлорангидридом фосфористой кислоты. Гидролиз её приводит к образованию двух кислот, а взаимодействие со щелочами — двух солей:
Полифосфорная кислота
|
Состав фосфорных кислот в зависимости от содержания в растворе Р2Об. |
Полифосфорные кислоты образуются при взаимодействии P2Os с ортофосфорной кислотой.
Полифосфорные кислоты, содержащие 77 — 86 % PsOs ( 106 — Л8 % Н3РО4), получают путем сжигания фосфора в футерованной шамотным кирпичом топке в токе первичного или вторичного воздуха и последующей гидратации и абсорбции паров фосфорного ангидрида в башне абсорбции. Процесс гидратации кислоты в башне происходит при температуре входящего газа 800 — 1000 С и кислоты, поступающей на орошение башни, около 115 С.
|
Строение молекулы. |
Полифосфорные кислоты легко образуют стекловидные фазы.
Полифосфорные кислоты способны также соединяться с микроэлементами почвы, переводя их в доступные для питания растений вещества.
Полифосфорная кислота в технике известна и под другими названиями. Кислоту, содержащую больше 72 4 % Р2О5, называют суперфосфорной. При 76 % Р2О5 она содержит 49 % Р2О5 в виде ортофосфорной, 42 % — в виде дифосфорной, 8 % — в виде триполифосфорной и 1 % — в виде тетр а полифосфор ной кислот. Плотность 76 % — й кислоты 1920 кг / м3, температура замерзания около О С.
Полифосфорная кислота в технике известна и под другими названиями. Кислоту с концентрацией 72 4 — 76 % Р2О5 называют суперфосфорной. Плотность 76 % — ной кислоты 1 92 г / см3, температура замерзания около О С.
|
Зависимость температуры кристаллизации полифос-фррной кислоты от содержания Р265. |
Полифосфорная кислота легко подвергается гидролизу, который может протекать даже под действием влаги воздуха.
Полифосфорные кислоты образуются при взаимодействии Р2О6 с ортофосфорной кислотой. Как видно из рис. 162, в системе Р205 — Н20 по мере увеличения содержания Р2О5 количество Н3РО4 уменьшается, а содержание полифосфорных кислот увеличивается.
Полифосфорные кислоты способны также соединяться с микроэлементами почвы, переводя их в доступные для питания растений вещества.
|
Соединение фосфоропроводов, обогреваемых горячей водой. / — фосфоропровод. 2 — канал для горячей воды. 3 — обходной канал. |
Полифосфорные кислоты отличаются низкой температурой замерзания.
Полифосфорная кислота в небольших количествах используется для производства высококонцентрированного суперфосфата с содержанием 54 — 55 % Р О Значительную часть экстракционной полифосфорной кислоты применяют для получения базисных ( основных) растворов состава 1О — 34 — О, используемых в производстве жидких комплексных удобрений. На основе термической полифосфорной кислоты получают базисные растворы состава 11 — 37 — О и суспендированные 12 — 40 — 0, которые также предназначаются для жидких удобрений.
Полифосфорная кислота
Полифосфорные кислоты отличаются низкой температурой замерзания. При обычной температуре они проявляют невысокую коррозионную активность и могут непродолжительное время храниться в емкостях из обычной углеродистой стали ( Ст. Продолжительность хранения ограничивается из-за высокой гигроскопичности полифосфорных кислот, поскольку при поглощении влаги из воздуха и разбавлении кислоты повышается скррость коррозии металла.
Полифосфорная кислота имеет и другие названия. Кислота с концентрацией 72 4 — 76 % Р205 называется суперфосфорной. При концентрации 76 % Р205 она содержит 49 % Р205 в виде ортофосфор-ной, 42 % — в виде пирофосфорной, 8 % — в виде триполифосфор-ной и 1 % — в виде тетраполифосфорной кислот.
Полифосфорная кислота, полученная нагреванием термической ортофосфорной кислоты с добавлением или без добавления фосфорного ангидрида, содержит орто -, поли -, пиро -, гекса — и метафосфорные кислоты. Полифосфорная кислота, полученная упариванием экстракционной фосфорной кислоты, кроме вышеперечисленных форм содержит примеси железа, алюминия, кальция, сульфатов, фтора и кремния.
Полифосфорная кислота содержит значительные количества дегидратированных кислот типа поли — и пиро-форм. Последние обладают свойством образовывать комплексные соединения с железом, алюминием и кальцием. Соответственно в системе имеется некоторое количество свободной воды. Гексаметафосфорная кислота образуется при содержании общей Р206 выше 82 %, при 89 % Р2О5 содержание ее достигает максимума. Метафосфорную кислоту находят по разности между общим содержанием Р205 и остальными формами кислот.
Полифосфорная кислота оказалась наилучшим циклизующим агентом для 4-амино — 5-ариламинопиримидинов ; 8-арилпурины получались высокой степени чистоты и с хорошими выходами.
Полифосфорные кислоты образуются при взаимодействии Р2О5 с ортофосфорной кислотой.
Полифосфорная кислота оказалась наилучшим циклизующим агентом для 4-амино — 5-ариламинопиримидинов ; 8-арилпурины получались высокой степени чистоты и с хорошими выходами.
Полифосфорные кислоты представляют собой высоковязкие жидкости, в которых наряду с линейными макромолекулами из связанных в цепи фосфатных тетраэдров содержатся низкомолекулярные циклические три -, тетра-и гексаметафосфаты.
|
Состав фосфорных кислот в зависимо — СаНР 4 — 2Н2О — преципи-сти от содержания в растворе Р2О5 тата. Смешанными азотно. |
Полифосфорные кислоты образуются при взаимодействии Р2О5 с ортофосфорной кислотой. Как видно из рис. 194, в системе Р2О6 — Н2О по мере увеличения содержания Р2О6 количество Н3РО4 уменьшается, а содержание полифосфорных кислот увеличивается.
Полифосфорная кислота может быть получена дегидратацией экстракционной фосфорной кислоты в процессе ее упаривания с выделением осадков или гидратацией P2Os — продукта сжигания.
Полифосфорные кислоты имеют но два концевых слабокислых гидро-ксила, другие же гидроксильные группы являются сильно кислыми. Полифосфорные кислоты представляют собой сиропы или кристаллические вещества.
Полифосфорная кислота, являющаяся сильной кислотой Льюиса, повышает реакционную способность электрофильного углеродного атома карбоксильной группы и вместе с тем действует как весьма энергичный дигид-ратирующий агент в реакции циклизации.
Полифосфорная кислота, в среде которой протекает эта реакция, повышает реакционную способность электрофильного углеродного атома карбонильной группы, а также являеятс дегидратирующим агентом для реакции отщепления воды, приводящей к образованию тиазольного цикла.
Полифосфорная кислота представляет собой смесь кислот различной степени гидратации P2Os и различной молекулярной структуры. Другие исследователи утверждают, что после установления равновесия они не обнаружили различия в составе полифосфорной кислоты, приготовленной выпариванием ортофосфорной кислоты, и кислоты, полученной насыщением ортофосфорной кислоты пятиокисью фосфора. Найдена кислота, строение которой пока точно не установлено. Кислота ( 79 — 80 % Р2О5) кристаллизуется при стоянии.
Что такое ортофосфорная кислота
При комнатной температуре это гигроскопичные бесцветные кристаллы ромбообразного вида, которые хорошо растворяются водой. Ортофосфорное соединение считается неорганической кислотой со средней силой. Одна из ее форм – желтоватая или бесцветная сиропообразная жидкость, без запаха, является водным раствором с концентрацией 85%. Другое ее название – белая фосфорная кислота.
Химическое ортофосфорное соединение имеет свойства:
- растворяется в этаноле, воде, растворителях;
- образует 3 ряда солей – фосфатов;
- вызывает ожоги при попадании на кожу;
- при взаимодействии с металлами образует горючий, взрывоопасный водород;
- температура кипения зависит от концентрации – от 103 до 380 градусов;
- жидкая форма склонна к переохлаждению;
- несовместимо с горючими материалами, чистыми металлами, негашеной известью, алкоголем, карбидом кальция, хлоратами;
- при температуре 42,35 градуса плавится, но не разлагается.

Химические свойства
При нагревании выше 300 °C практически полностью разлагается на PCl3 и Cl2. Степень диссоциации при 182 °C равна 41,7%, при 200°C 48,5%, при 250°C 80,0%, при 300°C 97,3%.
Пентахлорид фосфора — типичное кислотное соединение. Он энергично реагирует с водой, образуя по первой стадии оксохлорид фосфора(V):
-
- PCl5+H2O→POCl3+2HCl{\displaystyle {\mathsf {PCl_{5}+H_{2}O\rightarrow POCl_{3}+2HCl}}}
В горячей воде гидролиз протекает полностью, до образования ортофосфорной кислоты:
-
- PCl5+4H2O→H3PO4+5HCl{\displaystyle {\mathsf {PCl_{5}+4H_{2}O\rightarrow H_{3}PO_{4}+5HCl}}}
Для РCl5 характерны реакции окислительного хлорирования:
-
- PCl5+2NO2→PCl3+2NO2Cl{\displaystyle {\mathsf {PCl_{5}+2NO_{2}\rightarrow PCl_{3}+2NO_{2}Cl}}}
C концентрированной серной кислотой образует хлорсульфоновую кислоту:
-
- PCl5+H2SO4→ClSO2OH+POCl3+HCl{\displaystyle {\mathsf {PCl_{5}+H_{2}SO_{4}\rightarrow ClSO_{2}OH+POCl_{3}+HCl}}}
При нагревании РCl5 и NH4Cl происходит реакция образования полимера фосфонитрилхлорида:
-
- nPCl5+nNH4Cl→(PNCl2)n+4nHCl{\displaystyle n{\mathsf {PCl_{5}}}+n{\mathsf {NH_{4}Cl\rightarrow (PNCl_{2})}}_{n}+4n{\mathsf {HCl}}}
(PNCl2)n — прозрачное эластичное вещество, «неорганический каучук». Выдерживает нагревание выше 200 °C. Однако фосфонитрилхлорид сравнительно легко гидролизуется, что затрудняет его практическое использование. Заменой атомов хлора на органические радикалы можно получить водоустойчивые полимеры.
Пентахлорид фосфора является кислотой Льюиса.
Использование кислоты
Применение фосфорной кислоты достаточно широкое. Стоит рассмотреть наиболее популярные методы ее использования.
В медицине
Ее применяют в стоматологии во время пломбирования зубов для протравливания эмали непосредственно перед началом процесса. Эта процедура имеет свои негативные стороны, т. к. контролировать глубину и стадию расщепления эмали невозможно, как и их полное удаление перед пломбированием. Оставшееся после такой процедуры вещество может уменьшить прочность защиты и привести к образованию кислотных остатков на эмали зуба. Эта кислота добавляется в малых дозах в зубные отбеливатели.
Преимущество удаления ржавчины ортофосфорной кислотой состоит в том, что она убирает коррозию с металла и создает тонкую пленку на них, защищая от разных внешних воздействий. После покрытия этим веществом металлической поверхности начинается активный процесс разъедания и поглощения оксида железа. Затем на плоскости металла образуется серая пленка маслянистой консистенции.
Существуют различные методы удаления окислов, среди которых можно выделить следующие:
- с полным опусканием элемента в кислотный раствор;
- поверхностная обработка с использованием распылителя, кисти или валика;
- покрытие раствором предварительно обработанного механическим способом верхнего слоя металла.
Преобразователь коррозии — это кислотный раствор с различными добавками. Существуют такие виды растворов, в зависимости от используемых в их составе добавок:
- грунтовки;
- модификаторы-стабилизаторы;
- преобразователи ржавчины.
К 1 типу относится грунтовка ЭВА-0112, состоящая из основного компонента и 85% раствора вещества. Она выступает основой под покраску.
В состав преобразователя «Цинкарь» входит кислота и соли марганца и цинка. При его применении ржавчина трансформируется в плотный защитный слой. Происходит процесс легирования.
Ортофосфорная кислота для металла
Для очистки или для пайки металлических элементов необходимо проделать следующие операции. Перед полным погружением металлического элемента в ортофосфорный состав, его вначале зачищают от разных видов налета на поверхности, в частности от жиров. Для этого следует промыть деталь с использованием чистящего средства. После этого необходимо растворить 150 мл вещества в 1 л воды и опустить в этот раствор металлический элемент на 1 час, время от времени размешивая жидкость для большей эффективности.
Затем необходимо смыть смесь раствором, который состоит из 50% воды, 2% нашатырного спирта и 48% этанола. После этого элемент нужно ополоснуть под струей водой и хорошо высушить.
Перед тем как нанести распылитель на поверхность валиком или кистью, следует предварительно зачистить поверхность от ржавчины. После нанесения следует немного подождать, а затем смыть смесь нейтрализующим раствором и высушить деталь.
Применение в сельском хозяйстве
В сельском хозяйстве используют фосфорную кислоту, добытую из руды, в качестве удобрения. При попадании в грунт, а затем в растения, она помогает им перенести засуху и морозы. При этом почва становится более плодородной и благоприятной для выращивания овощных культур и зелени.
Применение кислоты в быту и пищевой промышленности
Применение кислоты в быту подразумевает ее использование для удаления коррозии с различных поверхностей (за исключением акриловых). Он подходит для обработки эмалированных и фаянсовых поверхностей. Перед нанесением раствора ортофосфорной кислоты металлическую поверхность необходимо обработать моющим средством. Для приготовления раствора следует смешать 1 л воды и 200 г действующего вещества, а затем нанести смесь на обрабатываемую плоскость на 1-12 часов. По прошествии времени смесь необходимо погасить содовым раствором и смыть.
В пищевом производстве применяется как регулятор кислотности.
Суперфосфорная кислота
Суперфосфорная кислота — это коммерческое название полифосфорных кислот, применяемое в химической промышленности. Насыщение полифосфорных кислот аммиаком производится под. Полифосфаты аммония хорошо растворяются в воде, а фосфор этих удобрений лучше усваивается растениями по сравнению с фосфатами. В виде жидкого комплексного удобрения используются полифосфаты аммония обычно с примесью фосфатов аммония. К нему добавляют нитрат или хлорид калия и получают тройное комплексное удобрение, а при необходимости добавляют микроэлементы и пестициды.
|
Требования к качеству простого суперфосфата. |
Суперфосфорная кислота, получаемая выпариванием экстракционной кислоты, применяется в производстве жидких комплексных азотно-фосфорных удобрений.
Суперфосфорная кислота — наиболее распространена из полифосфорных кислот. По аналогии с олеумом суперфосфорную кислоту называют также фосфолеу-мом. Но в отличие от олеума, она может быть получена не только растворением фосфорного ангидрида в ограниченном количестве воды, но и упариванием водных растворов фосфорной кислоты и ее дегидратацией.
Суперфосфорная кислота способна образовывать с примесями ( соединения железа и алюминия) растворимые комплексные соединения, что предотвращает ретроградацию фосфорного ангидрида в почве.
Суперфосфорная кислота в этом случае должна быть более концентрированная с повышенным содержанием Р205 в полиформе.
Суперфосфорная кислота, содержащая всего 0 1 — 0 3 % фтора, пригодна для производства кормовых фосфатов и изготовления зубных цементов. Обычно эти продукты получают из более дорогой термической кислоты.
|
Температуры кипения водных растворов фосфорной кислоты. |
Суперфосфорная кислота менее агрессивна по отношению к металлам и сплавам, чем ортофосфорная кислота, и является ценным сырьем для получения высококонцентрированных удобрений.
|
Диаграмма растворимости в системе Н3РО4 — Н2О. |
Суперфосфорная кислота с концентрацией 75 6 % Р2О5 содержит 49 % Р2О5 в виде ортофосфорной, 42 % — в виде пирофос-форной, 8 % в виде три-полифосфорной и 1 % — в виде тетраполифосфор-ной кислот. При разбавлении суперфосфорной кислоты водой происходит значительное выделение тепла и полифосфорные кислоты быстро гидратируются до ортофосфорной.
Суперфосфорная кислота содержит 70 — 80 % PzOs ( 96 — 110 % Н3РО4), при разбавлении ее водой происходит выделение тепла.
Суперфосфорная кислота, получаемая выпариванием экстракционной кислоты, находит применение в производстве жидких комплексных азотно-фосфорных удобрений ( стр.
Суперфосфорная кислота при концентрации Р2О5 около 70 % оказывает очень слабое коррозийное действие на обыкновенную углеродистую сталь. Увеличение или понижение концентрации такой кислоты резко усиливает коррозию малоуглеродистой стали.
Суперфосфорная кислота начинает применяться для получения более концентрированных, чем обычно, удобрений: жидких ( состава 11 — 36 — 0, см. гл.
Соль — метафосфорная кислота
Соль метафосфорной кислоты метафосфат натрия NaPO3 при сплавлении присоединяет оксиды некоторых металлов, получающиеся соли окрашены в различные цвета, чем пользуются в аналитической химии.
Соль метафосфорной кислоты — метафосфат натрия ЫаРОз при сплавлении присоединяет окислы некоторых металлов, меняет окраску в различные цвета, чем пользуются в аналитической химии.
Соли метафосфорной кислоты называются метафос-фатами. Некоторые из них растворимы в воде и существуют в полимерной форме. Основные и кислые соли полимерных кислот фосфора обычно получают реакцией поликонденсации с выделением воды, а также действием щелочей или аммиака на полимерные тела.
Некоторые соли отдельных метафосфорных кислот ( с определенными значениями п) были выделены в индивидуальном состоянии. Так, медленным взаимодействием фосфорного ангидрида с раствором соды на холоду может быть получен Na4P4Oi2 — 4H20 — Для триметафосфата натрия ( Ма3РзО9) известны кристаллогидраты с б и 1, для гекса-метафосфата ( NaePgOie) с 6 молекулами воды.
Некоторые соли отдельных метафосфорных кислот ( с определенными значениями п) были выделены в индивидуальном состоянии. Для триметафосфата натрия ( NasPA) известны кристаллогидраты с 6 и 1 молекулами воды.
На протяжении послевоенных лет началось экспериментальное производство солей метафосфорной кислоты, причем опытами доказано, что они являются пригодными для растений удобрениями. В этих условиях образуется жидкий метафосфат кальция — Са ( Р03) 2 — Охлаждаясь, он переходит в стекловидную массу, которую надо тонко размолоть.
В чем растворимы плохо растворимые в воде соли метафосфорной кислоты.
Метафосфорная кислота в чистом виде представляет собой стекловидную массу, легко растворимую в воде. Она одноосновная, следовательно, может образовать только средние соли. Соли метафосфорной кислоты называют метафосфатами, например NaP03 — метафосфат натрия.
Метафосфорные кислоты имеют общую формулу Н РпОзп, где п может принимать значения от 3 до 8; однако часто их состав выражают простейшей формулой НРОз — Эти кислоты представляют собой стеклообразные вещества. В раствор они переходят в виде полимеров, имеющих кольцевую структуру. С течением времени кольца расщепляются и образз ются цепные полифосфорные кислоты. Известны соли метафосфорных кислот — метафосфаты. Некоторые из них выделены в виде кристаллов, например NaaPsOg, Na4P40i2, Са3 ( РзОд) 2 — Метафосфаты применяются для умягчения воды и снижения ее коррозионной активности, для удаления накипи с паровых котлов, а также входят в состав некоторых моющих средств.
Метафосфорные кислоты имеют общую формулу HnPnO3n, где п может принимать значения от 3 до 8; однако часто их состав выражают простейшей формулой НРОз. Эти кислоты представляют собою стеклообразные вещества. В раствор они переходят в виде полимеров, имеющих кольцевую структуру. С течением времени кольца расщепляются и образуются цепные полифосфор-лые кислоты. Известны соли метафосфорных кислот — мет а фосфаты.
Ингибиторы коррозии, вводимые в жидкость для снижения ее агрессивности к металлам, являются весьма эффективным средством борьбы с коррозионными загрязнениями и широко используются в технике. Механизм действия ингибиторов коррозии заключается в создании на поверхности металла адсорбционной пленки поверхностно-активных веществ, которая вытесняет воду с этой поверхности и препятствует возникновению электрохимической коррозии. В качестве ингибитора коррозии используют непредельные жирные кислоты, оксикислоты и их эфиры, а также соли нефтяных сульфо-кислот, окисленный петролатум и другие вещества нефтяного происхождения, обладающие поверхностно-активными свойствами и образующие в жидкости мицеллярные растворы. Перспективным является применение для этой цели нитрованных масел, нейтрализованных гидратом оксида железа FeO. Перечисленные вещества нефтяного происхождения употребляются в качестве ингибиторов коррозии в водных растворах, в нефтепродуктах, в системах нефтепродукт — вода. Для предотвращения коррозии при контакте металла с неорганическими жидкостями ( например, серной, соляной и азотной кислотой) применяют вещества неорганического происхождения — соли метафосфорных кислот, оксиды азота, плавиковую кислоту и другие.